 |
| ||||||
Allmänt om...
Laddning
Mer om Batscan...
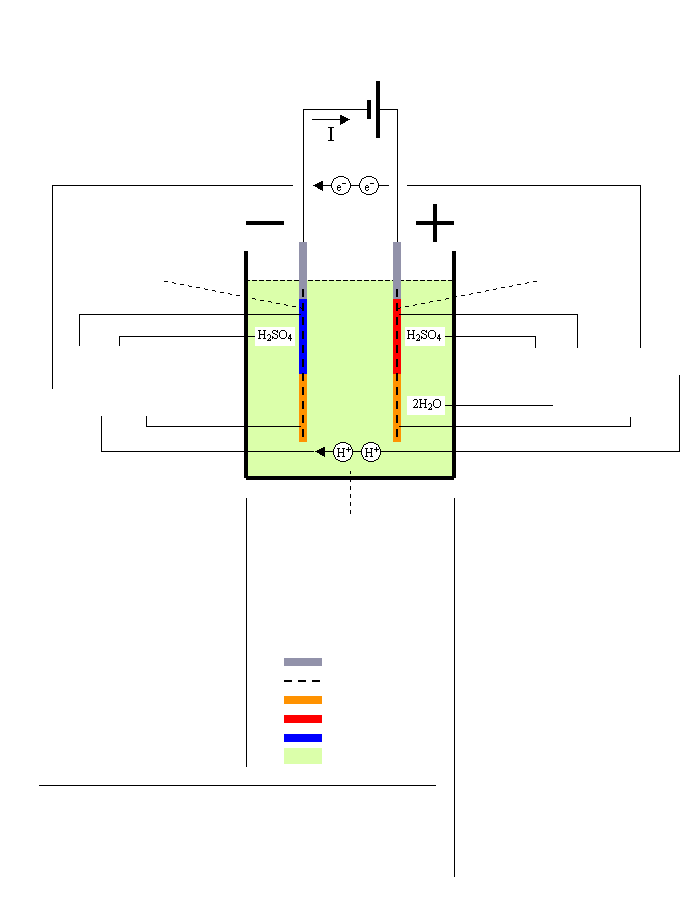
Laddning av Bly-Syra Batteri
Likströmskälla
Negativ platta = Katod
PbSO4 → Pb
Blysulfat → Blysvamp
PbSO4 → Pb
Blysulfat → Blysvamp
Pb + H2SO4
↑
[2e-] + 2H+ + PbSO4
↑
[2e-] + 2H+ + PbSO4
Reaktion vid -pol
(Reduktion)
(Reduktion)
| 1. |
De två tillförda elektronerna [2e-] reducerar blysulfaten som då delas upp
i en blyatom och en sulfatjon: [2e-] + PbSO4 → Pb + SO42- |
| 2. |
Sulfatjonen från [1] förenas med vätejonerna från [5] och bildar svavelsyra: 2H+ + SO42- → H2SO4 |
Elektrolyt = Svavelsyra
H2O → H2SO4
Vatten → Svavelsyra
H2O → H2SO4
Vatten → Svavelsyra
Blyelektroder
Gallerplatta
Blysulfat
Blydioxid
Blysvamp
Elektrolyt
Gallerplatta
Blysulfat
Blydioxid
Blysvamp
Elektrolyt
Nettoreaktion vid laddning
2PbSO4 + 2H2O → Pb + PbO2 + 2H2SO4
2Blysulfat + 2Vatten → Blysvamp + Blydioxid + 2Svavelsyra
(elektrisk energi → kemisk energi)
2PbSO4 + 2H2O → Pb + PbO2 + 2H2SO4
2Blysulfat + 2Vatten → Blysvamp + Blydioxid + 2Svavelsyra
(elektrisk energi → kemisk energi)
Positiv platta = Anod
PbSO4 → PbO2
Blysulfat → Blydioxid
PbSO4 → PbO2
Blysulfat → Blydioxid
H2SO4 + PbO2 + [2e-] + 2H+
↑
2H2O + PbSO4
↑
2H2O + PbSO4
Reaktion vid +pol
(Oxidation)
(Oxidation)
| 3. |
Genom att leda bort två elektroner [2e-] oxideras blysulfaten som då delas upp
i en blyjon(IV) och en sulfatjon: PbSO4 → [2e-] + Pb4+ + SO42- |
| 4. |
Sulfatjonen löses i vattnet och bildar svavelsyra varvid en syrejon frigörs: SO42- + H2O → H2SO4 + O2- |
| 5. |
Blyjonen från [3] förenas med syrejonen från [4] och en syreatom från vattnet
varvid två vätejoner frigörs till elektrolyten: |
|
Pb4+ + O2- + H2O → PbO2 + 2H+ |
|